Abb. 11.1.
Schema der Stufentherapie der Spastik in Abhängigkeit von Lokalisation und klinischer Ausprägung nach den Leitlinien der DGN
die orale Therapie,
die lokale Therapie, z. B. mit Botulinumtoxin (BTX), und
die intrathekale Baclofentherapie
unterschieden werden. Durch eine adäquate Behandlung der Spastik kann bei einem relevanten Teil der Patienten eine Funktionsverbesserung erreicht werden, und dadurch können z. B. Alltagsaktivitäten besser bewältigt werden. Zudem kann es zu einer Abnahme der Abhängigkeit von Pflegenden kommen. Insgesamt kann durch die Behandlung der Spastik eine signifikante Besserung der Lebensqualität erreicht werden (Ward et al. 2005; Wissel et al. 2009).
11.2 Orale antispastische Therapie
11.2.1 Zugelassene Medikamente
Die orale antispastische Therapie ist angezeigt, wenn eine Para- oder Tetraspastik vorliegt und nur geringe Restfunktionen erhalten sind:
Bei noch erhaltener Funktion z. B. im Sinne eines Gehens und/oder Stehens ist eine niedrige Dosierung zu empfehlen, um diese Funktionen nicht zu gefährden. Bei immobilen Patienten ist der Einsatz der Antispastika unproblematischer.
Bei einer fokalen umschriebenen Spastik ergibt sich selten eine Indikation für eine systemische Therapie, hier erscheint die lokale BTX-Injektion am geeignetsten. Zudem können zu hohe Dosierungen zu einer Zunahme des funktionellen Defizits führen.
Medikamente mit antispastischer Wirkung sind z. B. Baclofen, Dantrolen, Memantin, Phenothiazine, Diazepam, Tetrazepam und Tizanidin (Benecke 1987; Dietz u. Young 2003).
Die Angriffspunkte liegen spinal, supraspinal oder an den neuromuskulären Übertragungsstellen.
Baclofen
Baclofen ist ein Gamma-Amino-Buttersäure-Derivat, das selektiv am GABA-B-Rezeptor in den spinalen Hinterhörnern angreift; daher ist Baclofen besonders zur Behandlung der spinalen Spastik geeignet.
Tizanidin
Bei Tizanidin handelt es sich um eine alpha-2-adrenerge Substanz, die spinale und supraspinale Angriffspunkte hat.
Tetrazepam
Tetrazepam wirkt als Neuromodulator am GABA-A-Rezeptor, Interneurone werden über eine postsynaptische Hyperpolarisation inhibiert.
Tolperison
Bei Tolperison ist der Wirkmechanismus nicht genau bekannt, die Wirkung entfaltet sich auf zentraler und peripherer Ebene als Kanalblocker; daher darf keine Anwendung bei Patienten mit Myasthenia gravis erfolgen.
Dantrolen
Dantrolen wirkt – im Gegensatz zu den vorherig genannten Präparaten – rein peripher durch Beeinflussung spannungsabhängiger Ca2+-Kanäle im Muskel.
Entsprechend den Leitlinien der DGN werden Baclofen und Tizanidin wegen der tolerablen Nebenwirkungen und des geringen sedierenden Effekts als Mittel der 1. Wahl angesehen (Dietz et al. 2008).
Dosierung, Nebenwirkungen, Kontraindikationen
Bei Patienten, die neben der Spastik an Unruhezuständen leiden, können die Nebenwirkungen gleichzeitig zur Behandlung dieser genutzt werden, z. B. im Fall von Benzodiazepinen. In der Regel wird eine einschleichende Dosierung empfohlen, damit möglicherweise vorhandene Restfunktionen wie Transfer-, Steh- oder Gehfähigkeit nicht beeinträchtigt werden.
Empfehlungen zu Dosierungen, wichtigen Nebenwirkungen und Kontraindikationen für die oralen Antispastika Baclofen, Tizanidin, Tetrazepam, Tolperison und Dantrolen sind in ◘ Tab. 11.1 aufgeführt, wobei diese keinen Anspruch auf Vollständigkeit erheben. Generell ist bei Schwangerschaft und Stillzeit auf die expliziten Hinweise der Hersteller besonders zu achten.
Tab. 11.1.
Wichtige Wirkstoffe zur Spastikbehandlung sowie deren Dosierungen, wichtige Nebenwirkungen und Kontraindikationen
Wirkstoff (Generika) | Dosierung | Wichtige Nebenwirkungen | Kontraindikationen | Hinweise |
|---|---|---|---|---|
Baclofen (Baclofen AWD®, Baclofen ratiopharm®, Lebic®, Lioresal®) | Initial 3×5 mg, Steigerung alle 3 Tage um 5 mg; max. 150 mg/Tag Beendigung: Ausschleichen über 3 Wochen | Schläfrigkeit, Sedation, v. a. zu Beginn der Behandlung, Benommenheit, Schwindel, Ataxie, Blutdruckabfall u. a. | Epilepsien, Parkinsonismus, terminale Niereninsuffizienz Cave: Bei Leberfunktionsstörungen, Magen-Darm-Ulzera | Besonders bei spinaler Spastikform wirksam |
Tizanidin (Sirdalud®, Tizanidin Teva®) | Initial abends 2 mg, Steigerung alle 5 Tage um 2 mg auf 3×2 mg, nach Wirkung und NW steigern bis auf max. 36 mg/Tag | Schläfrigkeit, Müdigkeit, Schwindel, Mundtrockenheit, Blutdruckabfall, Bradykardie u. a. | Myasthenia gravis, Epilepsie, Herz-Kreislauf-Insuffizienz Cave: Dosisreduktion bei eingeschränkter Leber- oder Nierenfunktion | Bei allen Formen der Spastik einsetzbar |
Tetrazepam (Musapam®, Musaril®, Myospasmal®, Rilex®, Tetramdura®, Tetrazepam ratiopharm® u. a.) | Initial 50 mg/Tag, Steigerung um 25 mg/Tag nach Wirksamkeit Übliche Dosen: 50–200 mg/Tag; max. 400 mg/Tag Bei abruptem Absetzen Gefahr eines Entzugssyndroms | Schläfrigkeit, Benommenheit, Mattigkeit, Schwindel, Artikulationsstörungen, Hautallergien u. a. | Schwere Leberschäden, schwere respiratorische Insuffizienz, Schlafapnoe-Syndrom, Engwinkelglaukom Cave: Toleranzentwicklung und Gefahr der Abhängigkeit bei längerer Anwendung; daher bei Medikamenten-, Drogen- oder Alkoholabhängigkeit nur bei zwingender Indikation | Einsatz in der Kurzzeittherapie (wegen NW und Abhängigkeitspotenzial), z. B. bei schmerzhaften Spasmen |
Tolperison (Mydocalm®, Tolperison HEXAL®, Viveo®) | 3×50 mg bis max. 3×150 mg/Tag | Nebenwirkungsarm, gelegentlich Schwindel, Schläfrigkeit, Kopfschmerzen; selten Darmbeschwerden, Exanthem u. a. | Myasthenia gravis | Gut verträglich, wird häufig bei Muskelverspannungen und schmerzhaften Spasmen eingesetzt |
Dantrolen (Dantamacrin®, Dantrium®) | Initial (1. Woche) 2×25 mg/Tag, 2. Woche 4×25 mg/Tag, 3. Woche 3×50 mg/Tag, 4. Woche 4×50 mg/Tag Übliche Dosen: 200 mg/Tag, max. 400 mg/Tag | Müdigkeit, Schwächegefühl, allg. Unwohlsein, Schwindel, Benommenheit, Durchfall, Kopfschmerzen, Störungen der Leber und Galle u. a. | Lebererkrankungen, eingeschränkte Lungenfunktion, schwere Herzmuskelschäden CAVE: Bei amyotropher Lateralsklerose, bulbärparalytische Symptome können verstärkt werden Hinweis: Vor und während der Therapie Kontrolle der Leberenzyme | Einsatz nur unter strenger Indikationsstellung, engmaschige Leberwertkontrollen empfohlen |
11.2.2 Cannabinoide
Cannabinoide wie Marinol® oder Cesamet® sind in Deutschland nicht zugelassen und nur über die internationale Apotheke zu beziehen. Im Tierversuch konnte eine antispastische Wirkung nachgewiesen werden; dieser Effekt auf die Spastik konnte in einer Studie mit Patienten mit Multipler Sklerose nicht reproduziert werden, allerdings wurde eine Besserung der Schmerzen und der Mobilität beobachtet (Zajicek et al. 2003).
Seit Juli 2011 ist nun das Cannabinoid Sativex® in Deutschland bei Spastik als Zusatzbehandlung für eine Verbesserung von Symptomen bei Patienten mit mittelschwerer bis schwerer Spastik aufgrund von Multipler Sklerose (MS), die nicht angemessen auf eine andere antispastische Arzneimitteltherapie angesprochen haben, zugelassen.
Das Präparat steht als Spray zur Anwendung in der Mundhöhle zur Verfügung. Vom Hersteller wird eine Titrationsphase von 14 Tagen empfohlen, das Ansprechen des Patienten auf Sativex® sollte nach 4 Wochen Behandlung überprüft werden. In diesem Zeitraum sollte sich eine erhebliche klinische Verbesserung von mit der Spastik verbundenen Symptomen zeigen, ansonsten sollte die Behandlung laut Fachinformation beendet werden. Die häufigsten berichteten Nebenwirkungen in den ersten 4 Wochen der Exposition waren Schwindelanfälle, die hauptsächlich während der Anfangstitrationsphase auftreten, und Müdigkeit. Diese Reaktionen sind laut Fachinformation üblicherweise schwach bis mäßig und werden nach einigen Tagen weniger, selbst wenn die Behandlung fortgeführt wird. Da es unter der Behandlung mit Sativex® zu Palpitationen und Tachykardien kommen kann, wird die Anwendung bei Patienten mit einer schweren Herz-Kreislauf-Erkrankung nicht empfohlen. Bei Vorliegen einer Schizophrenie oder einer anderen psychotischen Krankheit (auch in der Familienanamnese) bzw. bestimmter psychiatrischer Krankheiten ist die Anwendung kontraindiziert.
11.2.3 L-Dopa/Gabapentin
Für L-Dopa und Gabapentin wurden in kleinen Patientengruppen antispastische Effekte beschrieben. Beide Präparate sind aber für die Spastikbehandlung nicht zugelassen.
11.3 Botulinumtoxintherapie
Die BTX-Therapie ist eine elegante Methode zur Spastikbehandlung, da durch die Injektionen eine lokale Tonussenkung erreicht werden kann. Die Nebenwirkungsraten sind sehr gering, und die BTX-Therapie ist mit anderen Therapieansätzen wie Redression, physikalische Therapie, klassische Bewegungstherapie und neuromodulatorischen Therapien kombinierbar. Heutzutage wird die Behandlung im multidisziplinären Team empfohlen, bestehend aus Neurologen, Rehabilitationsmedizinern, Neurochirurgen, Orthopäden sowie Physio- und Ergotherapeuten. In diesem multiprofesionellen Behandlungsansatz sollen die zur Verfügung stehenden Therapien optimal genutzt werden. Um dies zu erreichen, werden gemeinsame Fallkonferenzen in einem Shared-Care-Ansatz empfohlen. Insbesondere in der ambulanten Versorgung von Spastikpatienten ist dies aufgrund der ungenügenden Abbildung in den Bewertungs- und Vergütungssystemen bisher nur unzureichend etabliert (Wissel et al. 2011).
11.3.1 Wirkungsweise, Wirkeintritt und Wirkdauer
BTX wirkt an der neuromuskulären Endplatte, indem es durch eine reversible Blockade die Freisetzung von Acetylcholin aus der terminalen Synapse verhindert. Aus der temporären Unterbrechung der neuromuskulären Übertragung resultiert eine vorübergehende Schwächung der injizierten Muskulatur. Die Wirkung des BTX tritt i. d. R. nach 3–5 Tagen ein und hält für 10–12 Wochen an. Eine Reinjektion sollte frühestens nach 8 Wochen erfolgen, um die Gefahr der Bildung von neutralisierenden Antikörpern zu minimieren. Diese können zu einer sekundären Non-Response führen. Insgesamt ist die Antikörperbildungsrate als sehr niedrig anzusehen; sie liegt auch in Langzeitstudien im einstelligen Prozentbereich, in unserem Patientengut bei unter 3 % (Kollewe et al. 2010; Mohammadi et al. 2009, 2010).
11.3.2 Medikamente
Zum aktuellen Zeitpunkt sind die Botulinumtoxin-A-Präparate
Botox®,
Dysport® und
Xeomin®
für die Spastik der oberen Extremität bei Schlaganfallpatienten im Erwachsenenalter zugelassen und dies nur für bestimmte Muskeln (◘ Tab. 11.2). Botulinumtoxin Typ B hat zum aktuellen Zeitpunkt keine Zulassung zur Injektion bei Spastik. Die meisten Untersuchungen und Studien bzgl. Botulinumtoxin-A-Behandlungen bei Spastik wurden aus diesem Grunde in den oberen Extremitäten vornehmlich bei Spastik nach Schlaganfall durchgeführt. Natürlich ist die BTX-Therapie auch bei Spastik anderer Ätiologie wie z. B. Zustand nach anoxischen, toxischen oder metabolischen Enzephalopathien, bei Multipler Sklerose, Tumoren, Abszessen, Zysten oder nach Trauma wirksam (Mohammadi et al. 2010).
Tab. 11.2.
Zulassungsstatus von Botulinumtoxin A bei Spastik
Botulinumtoxin A | Spastik | Muskeln |
|---|---|---|
Botox® | Fokale Spastizität – mit Spitzfußstellung bei ICP–Patienten >2 Jahre (max. 200 MU pro Sitzung) – des Handgelenks und der Hand bei erwachsenen Schlaganfallpatienten (bis max. 240 MU pro Sitzung) | – M. flex. dig. profondus – M. flex. dig. sublimis – M. flex. carpi radialis – M. flex. carpi ulnaris – M. add. pollicis – M. flex. pollicis longus |
Dysport® | Armspastik bei Erwachsenen infolge eines Schlaganfalls bis max. 1000 MU pro Sitzung | – M. biceps brachii – M. flex. dig. profundus – M. flex. dig. superficialis – M. flex. carpi ulnaris – M. flex. carpi radialis |
Xeomin® | Spastik der oberen Extremitäten nach Schlaganfall mit Handgelenkbeugung und gefausteter Hand bis 400 MU pro Sitzung | – M. flex. dig. superficialis – M. flex. dig. profundus – M. flex. carpi radialis – M. flex. carpi ulnaris – M. brachioradialis – M. biceps brachii – M. brachialis – M. pronator quadratus – M. pronator teres – M. flexor pollicis longus – M. adductor pollicis – Mm. flexor pollicis brevis/opponens pollicis |
Die Behandlung von spastischen Muskeln der oberen Extremitäten anderer Ätiologie als nach einem Schlaganfall bzw. der unteren Extremitäten stellt derzeit in Deutschland einen sog. Off-label Use dar.
Juristisch geht bei einem Off-label Use die Haftung auf den injizierenden Arzt über. Somit entstehen umfangreiche Aufklärungs- und Einwilligungspflichten. Der administrative Aufwand bei Off-label Use ist deutlich erhöht, obwohl BTX unabhängig von der Ätiologie und Lokalisation auf überaktive Muskeln wirkt und somit die Beschränkungen wissenschaftlich nicht nachvollziehbar sind (Wissel et al. 2011).
11.3.2.1 Zubereitung der Medikamente
Es stehen die o. g. Darreichungsformen vom Serotyp A zur Verfügung – Botox®, Dysport® und Xeomin® (◘ Abb. 11.2):
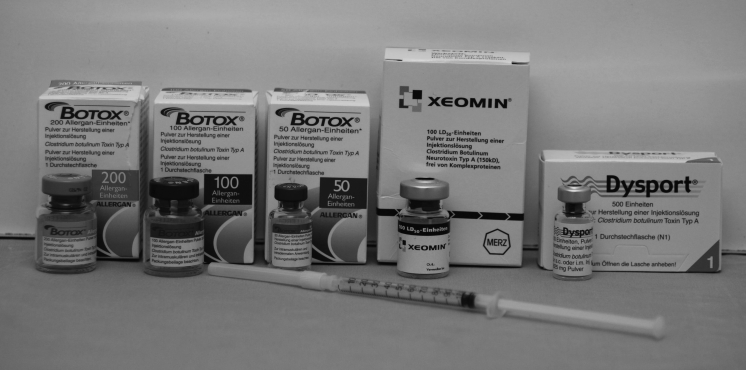

Abb. 11.2.
Aktuell verfügbare Botulinumtoxin-A-Präparate
Bei Botox® sind inzwischen 3 verschiedene Ampullengrößen erhältlich (50 MU, 100 MU, 200 MU).
Bei Xeomin® stehen 2 verschiedene Ampullengrößen mit 50 und 100 MU zur Verfügung.
Bei Dysport® enthält eine Ampulle 500 MU.
Bei Dosierungsempfehlungen muss immer darauf geachtet werden, auf welches Toxin sich diese beziehen. Aus unserer Erfahrung können Xeomin® und Botox® im Verhältnis 1:1 verwendet werden. Der Konversionsfaktor zwischen Botox® und Dysport® wird in der Literatur zwischen 1:2 und 1:6 (Hambleton u. Pickett 1994) angegeben. Entsprechend unserer Erfahrung und Auswertung eigener Behandlungsdaten (Kollewe et al. 2010; Mohammadi et al. 2009, 2010) benutzen wir einen Umrechnungsfaktor bis 1:3.
Die Herstellung der Injektionslösung erfolgt bei allen Darreichungsformen unter Zugabe physiologischer Kochsalzlösung zur Trockensubstanz:
Bei Dysport® wird die Zugabe von 2,5 ml auf das Vial mit 500 MU in der Fachinformation empfohlen, wodurch eine klare Lösung mit 200 MU pro 1 ml entsteht.
Bei Xeomin® werden Zugaben von 0,5–8 ml auf ein 100-MU-Vial angegeben.
Bei Botox® finden sich keine Angaben zur Verdünnung.
Wir verwenden in unserer BTX-Ambulanz bei Botox® und Xeomin® die Zugabe von 2,5 ml Kochsalzlösung auf ein 100-MU-Vial, so dass eine Konzentration von 40 MU pro Milliliter entsteht.
Die gebrauchsfertige Lösung sollte sofort verwendet werden,
bei Dysport® kann laut Hersteller eine Lagerung bei 2–8 °C für maximal 8 Stunden erfolgen,
bei Botox® und Xeomin® bei selbiger Temperatur bis zu 24 Stunden.
11.3.3 Nebenwirkungen der BTX-Therapie
Nebenwirkungen der BTX-Therapie sind aus Erfahrung der Autoren selten und liegen nach Auswertung eigener Behandlungsdaten bei der Behandlung der Spastik im einstelligen Prozentbereich (<4 %). Generell kann man davon ausgehen, dass die unerwünschte Wirkung nur vorübergehend besteht und sich schneller zurückbildet als die gewünschte Wirkung. Systemische oder schwerwiegende Nebenwirkungen werden noch seltener berichtet. In Langzeitstudien über bis zu 12 Jahren wird nicht über zusätzliche Nebenwirkungen berichtet (Kollewe et al. 2010; Mohammadi et al. 2009, 2010). Mögliche Nebenwirkungen werden in ▶ Übersicht 11.1 beschrieben. Nach unserer Erfahrung treten am häufigsten eine Muskelschwäche im Bereich der injizierten Muskeln, Schmerzen und Hämatome an der Injektionsstelle auf, systemische Nebenwirkungen wurden nur in Ausnahmefällen rückgemeldet und betrafen dann eine vorübergehende erhöhte Ermüdbarkeit.
Übersicht 11.1. Nebenwirkungen der BTX-Therapie
Häufig (1 bis 10 Behandelte von 100):
Muskelschwäche im Bereich der injizierten Muskeln
Hämatom, Schmerzen, Brennen an der Injektionsstelle
Grippeähnliche Symptome, Ermüdung
Selten (1 bis 10 Behandelte von 10.000):
Hautrötung an der Injektionsstelle
Schwindel
Sehr selten (<1 Behandelter von 10.000):
Allgemeine Muskelschwäche
Schluckstörungen
(Nicht alle in der Literatur beschriebenen Nebenwirkungen sind aufgelistet, die Angaben zu den Häufigkeiten schwanken bei den verschiedenen Herstellern.)
11.3.4 Kontraindikationen der BTX-Therapie
Kontraindikationen einer BTX-Therapie liegen bei neuromuskulären Erkrankungen und betreffen ansonsten hauptsächlich Kontraindikationen für eine intramuskuläre Injektion (Infektionen an der Injektionsstelle, Gerinnungsstörungen, orale Antikoagulation) sowie diejenigen für eine Medikamentengabe an sich (Schwangerschaft, Stillzeit). Weitere Kontraindikationen sind in ▶ Übersicht 11.2 aufgelistet.
Übersicht 11.2. Absolute und relative Kontraindikationen der BTX-Therapie
Absolute Kontraindikationen:
Neuromuskuläre Erkrankungen (Myasthenia gravis, Lambert-Eaton-Syndrom, amyotrophe Lateralsklerose)
Knöcherne Kontrakturen
Infektionen der zu injizierenden Muskulatur
Gabe von Aminoglykosiden
Schwere Gerinnungsstörungen
Unverträglichkeit gegen BTX
Schwangerschaft
Stillperiode
Relative Kontraindikationen:
Orale Antikoagulation
Schwere Formen der Dysphagie
Krankheiten mit hohem Aspirationsrisiko
Die orale Antikoagulation stellt eine relative Kontraindikation dar: Wir injizieren bei einem Quick-Wert über 50 %. Dabei sollte zudem beachtet werden, dass man die injizierte Muskulatur ggf. ausreichend komprimieren kann. Ebenso stellt die gleichzeitige Anwendung von Aminoglykosiden ein Risiko dar, da die Wirkung des BTX verstärkt werden kann; eine Behandlung wird daher erst 3 Tage nach Antibiotikagabe empfohlen.
Auch bei bekannten Wiedervorstellungen immer die Kontraindikationen vor der Injektion abfragen, besonders die Einnahme von oralen Antikoagulanzien und Thrombozytenaggregationshemmern, die Patienten mit einer Spastik als Folge eines Schlaganfalls häufig verordnet werden.
11.3.5 Formulierung der Ziele
Nach Überprüfung von möglichen Kontraindikationen und Aufklärung über das Wesen der BTX-Therapie und möglicher Nebenwirkungen kann die Injektion erfolgen.
Die Auswahl der Muskeln erfolgt nach der klinischen Untersuchung und ggf. basierend auf der Elektromyographie. Zudem sollte die spontane Fehlhaltung in die Beurteilung miteinfließen. Die Zielvereinbarung der BTX-Therapie sollte gemeinsam mit dem Patienten und ggf. mit dessen Angehörigen erfolgen. Diese sollten realistisch sein; es ist häufig so, dass sich die Patienten von den Injektionen eine Wiederherstellung ihrer Kraft erwarten. Diese Erwartung sollte man konkret thematisieren und darauf hinweisen, dass dies nicht möglich ist. Realistische Therapieziele können sein:
Hygiene-/Pflegeerleichterung,
Schmerzreduktion,
Funktionsverbesserung,
Behandlung und Prävention von Sekundärulzera wie Druckulzera und Ortheseintoleranz.
Eine geeignete Skala ist die Goal Attainment Scale, bei der Individualziele semiquantitativ dargestellt werden können (Wissel et al. 2011).
11.3.6 Dosierung
Entsprechend des 10-Punkte-Konsensus 2010 liegt die empfohlene Höchstdosis für jeweils die obere und untere Extremität bei
1000 MU für Dysport® und
500 MU für Botox® bzw. Xeomin®.
Pro Injektionsstelle sollten nicht mehr als 125 MU Dysport® bzw. 50 MU Botox® bzw. Xeomin® injiziert werden. Die Gesamtdosis pro Injektionssitzung sollte 1500 MU Dysport® bzw. 600 MU Botox® bzw. Xeomin® nicht überschreiten (Wissel et al. 2011).
Zum Überblick sei in ▶ Übersicht 11.3 nochmals das Prozedere einer BTX-Behandlung dargestellt.
Übersicht 11.3. Prozedere einer BTX-Behandlung
1.
Prüfung der Indikation zur Injektion
2.
Zielformulierung
3.
Prüfung der Kontraindikationen
4.
Aufklärung des Patienten
5.
Festlegung des Injektionsschemas
6.
Zubereitung des Medikaments
7.
Desinfektion
8.
Injektion
9.
Termin zur Wiedervorstellung vereinbaren
11.3.7 Praktisches Vorgehen
Im Folgenden werden exemplarisch häufige Spastikmuster der oberen bzw. unteren Extremität ausgewählt und aufgelistet. Die jeweils betroffenen Muskeln sind in den entsprechenden Tabellen aufgelistet, wobei weniger häufig betroffene Muskeln mit einem [*] gekennzeichnet sind, in Anlehnung an den „Therapieleitfaden Spastik – Dystonien“ (Reichel 2009) und „Neuroanatomie der Muskulatur bei Extremitätenspastik“ (Reichel 2010). Dosierungen sind für die Botulinumtoxin Typ A-Präparate Dysport®, Botox® und Xeomin® angegeben, wobei es sich hier nur um Anhaltswerte in Anlehnung an den „Bildatlas der Botulinumtoxin-Injektion“ (Jost 2009) handelt. Die maximalen Höchstdosen pro Injektionssitzung müssen beachtet werden. Für Angaben über Dosierungsanweisungen kann keine Gewähr übernommen werden. Jede Dosierung und Applikation erfolgt in eigener Verantwortung des Benutzers.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree








